本期文章将将为您介绍IQOQ。
IQOQ在研究和制造领域是一个耳熟能详的术语。
最近,这一需求已被纳入医药产品销售流程(GDP)指南。
例如,药品“仓库”也作为IQOQ进行“温度分布图”。
此外,还要求批发商“正确进行IQOQ”,以确保正确安装和按要求正确操作。
亚速旺公司负责的各种设备在安装时也可由专人进行IQOQ (^▽^)。
很多人似乎都知道“IQOQ”,但很多人对它的了解都稍显不足。
所以,
“IQOQ到底是什么?”
“也就是验证,对吧?”
“什么时候进行?”
我们通过类似种种问题,带您进入此次对于IQOQ的介绍。
进行IQ、OQ和PQ,也称为“资格检查”。
每一项都有这样的含义。
● IQ(Installation Qualification,安装资格确认)
→检查并记录仪器、测量设备和生产设施等设备的正确安装和运行是否符合规格书。
● OQ(Operational Qualification,操作资格确认)
→检查并记录仪器、测量设备和生产设施等设备是否按规格书要求达到预期能力。
● PQ(Performance Qualification,性能资格评价)
→确认并记录设备及相关辅助设备和系统能够按照批准的制造方法和标准有效运行并可重复使用。
听起来很复杂。
大致图像是这样的↓示意图↓
【IQ】产品是否齐全?是否发生损坏?是否正确安装?
【OQ】能否正常工作?数值是否正常?准度如何?
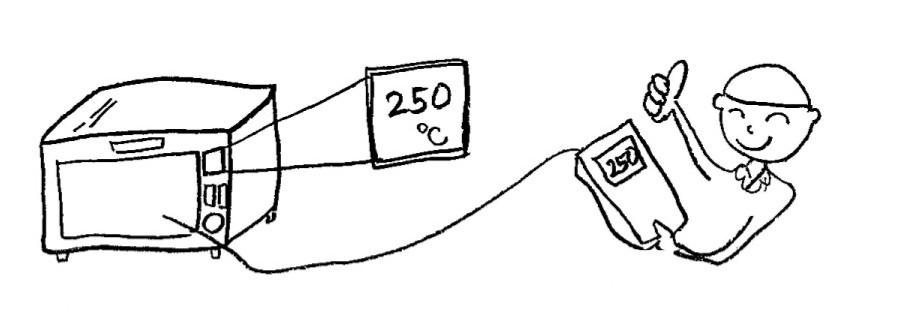
【PQ】其能力是否满足预计效果?
即使产品在完工后经过制造商检验,在装运和安装之间仍可能出现缺陷。
因此,只有在检查设备的安装状态时,我们才将其视为“具有原始用途的设备”。
“安装完成的状态”需要检查是否能正常运转。
在OQ中“空载”是试运行。如果是用干燥器,则是“在里面什么都没有”的情况下加热干燥器,然后进行检查。
在PQ中“有负载”就是以实际使用的方式运行。如果使用干燥器,则将目标样本放入干燥器中加热。
通常的做法是在产品推出时进行IQ和OQ,在产品投入使用后定期进行PQ。
通过持续定期实施PQ确认运行状况,可确保运行符合其初衷。
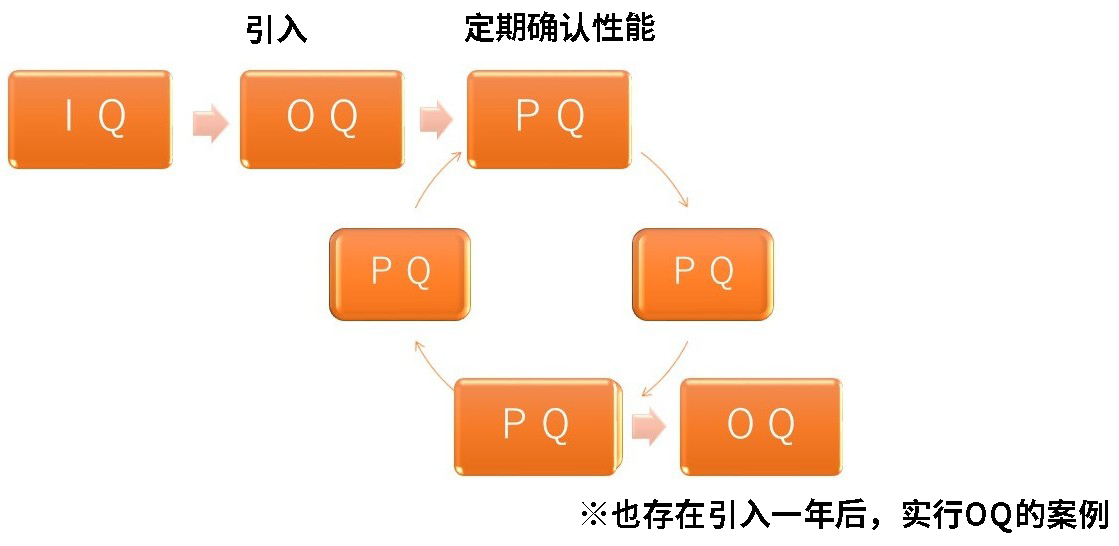
通过这种方式进行IQOQ,并在使用时定期进行PQ,
就能实现“我们使用的设备都能发挥其应有的性能!”
GMP等准则还要求对药品生产和质量控制场所进行IQOQ和验证等管理。
执行和记录一系列检查的过程称为验证。
※验证=validation,基本含义是核查、有效性等。
“我们要为哪种产品实施?”
“我们要进行什么内容?”
“什么时候做”
设备制造商并无这些义务进行。
这取决于“用户”。
一般来说,用户都按照各自的准则进行,如GMP。
在搬迁设备时也会验证。
亚速旺公司则是按照这一过程进行推进
【实际流程】
指定对象设备提交报价单
↓
委托
↓
提交计划(按照客户指定的格式,如有)。
↓
内容检查,必要时重新提交报价单和计划书
↓
签署计划书
↓
实施IQ/OQ

↓
制定文件

↓
提交
以下是最常申请IQOQ的产品组列表。
干燥器(恒温箱)

培养箱

水浴

天平

大多数委托是“温度控制”设备。
最后,向您介绍一种便于检查日常温度的记录仪。
12ch类型非常适合同时测量12个待测点。

产品引进时的IQOQ~运营时,日常检查中的PQ等,亚速旺公司将根据客户情况进行验证。
如有委托和查询,请联系我们!